Install the app
How to install the app on iOS
Follow along with the video below to see how to install our site as a web app on your home screen.
Nota: This feature may not be available in some browsers.
Estás usando un navegador desactualizado. Es posible que no muestre este u otros sitios web correctamente.
Debe actualizar o usar un navegador alternativo.
Debe actualizar o usar un navegador alternativo.
*Tema mítico* : ⚡⚡(HILO OFICIAL) : CRISIS DEL cobi19 ☣SARS-CoV2☣
- Autor del tema ULTRAPACO
- Fecha de inicio
El exclavizador de mentes
Será en Octubre
Y si el truco es enfermar?
Recuerdo la película de Guerra Mundial Z, cuando descubrieron que los zombies no atacaban a los enfermos y los esquivaban.
Si tenemos en cuenta que dicen que la hidroxicloroquina da muy buenos resultados a los pacientes, porque se usa para contrarestar el empuje de nuestro sistema inmunológico, pregunto yo..
Existe alguna forma de debilitar nuestro sistema inmunológico para que no reaccione tan fuerte al bichito?
⚡(HILO OFICIAL) : CRISIS DEL cobi19 ☣cobi19☣
Victor Chanov
Madmaxista
LoQueNoCuentan
Será en Octubre
- Desde
- 15 Abr 2012
- Mensajes
- 31.916
- Reputación
- 28.196
La gente que llama a esto dictadura no saben que existen los estados de alarma, sitio y excepción?
al loro
Madmaxista
- Desde
- 30 May 2012
- Mensajes
- 22.601
- Reputación
- 36.496
La hidroxicloroquina, si te pasas de dosis durante mucho tiempo, da pérdida visual.
Hidroxicloroquina (Plaquenil)
Hidroxicloroquina (Plaquenil)
La hidroxicloroquina, por lo general, se tolera muy bien y los efectos secundarios graves son poco frecuentes. Los efectos secundarios más comunes son náuseas y diarrea, que suelen mejorar con el tiempo o al tomar el medicamento con las comidas. Entre los efectos secundarios menos comunes se encuentran erupciones cutáneas, cambios en el pigmento de la piel (como oscurecimiento o puntos neցros), en el cabello (decoloración o fragilidad) y debilidad muscular.
En muy pocos casos, la hidroxicloroquina puede provocar anemia en algunos pacientes. Esto puede suceder en personas con una afección conocida como deficiencia de G6PD o porfiria.
En casos poco frecuentes, la hidroxicloroquina ha causado trastornos visuales o pérdida de la visión, pero estos problemas se producen con mayor frecuencia en los pacientes que toman dosis altas durante muchos años, en personas de 60 años o mayores, o en los que sufren enfermedades renales considerables. La dosis utilizada hoy en día es menor que la que se empleaba originalmente para tratar la artritis o malaria. En la dosis actual recomendada, es muy improbable que se presenten problemas visuales durante el tratamiento con este medicamento.
En muy pocos casos, la hidroxicloroquina puede provocar anemia en algunos pacientes. Esto puede suceder en personas con una afección conocida como deficiencia de G6PD o porfiria.
En casos poco frecuentes, la hidroxicloroquina ha causado trastornos visuales o pérdida de la visión, pero estos problemas se producen con mayor frecuencia en los pacientes que toman dosis altas durante muchos años, en personas de 60 años o mayores, o en los que sufren enfermedades renales considerables. La dosis utilizada hoy en día es menor que la que se empleaba originalmente para tratar la artritis o malaria. En la dosis actual recomendada, es muy improbable que se presenten problemas visuales durante el tratamiento con este medicamento.
tunante
Madmaxista
- Desde
- 7 Jul 2006
- Mensajes
- 7.321
- Reputación
- 15.861
Pero, ¿qué cosa de comportamiento es ese?
¿Qué narices está pasando ahí?
que están echandolo?
El idiota
Himbersor
- Desde
- 25 Nov 2019
- Mensajes
- 4.938
- Reputación
- 6.015
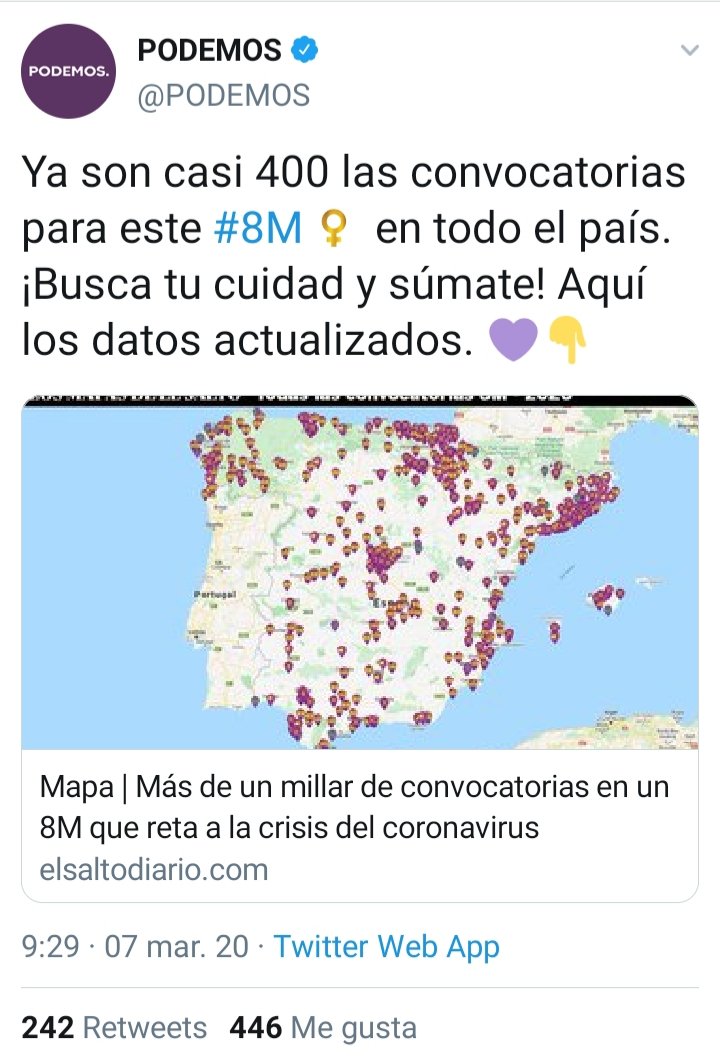
El problema,es que el bobiernocon su CNI y su Inteligencia militar, arengo a la masa a salir en tromba el 8m. Por esa razón desoyó todas las alarmas que les avisaban de lo que se venia encima. Este gobierno es responsable directo de todo lo que está pasando y de lo que está por venir. Mira a tu derecha y a tu izquierda. En 12 meses uno de los tres no estará.
Me parece bien los cansinos que estais el 8 m, me pregunto que diran de todos los contagios de Italia, francia, alemania o uk, a que ente maligno le echaran la culpa.
METRO Y BUSES, focos de infeccion
Pues viendo eso y las convocatorias, .en algunas zonas como galicia has docenas y docenas ( por si no lo sabeis en galicia son muy femisnistas) y al norte de vitoria las feministas vascas son mucho mas fuertes que en el sur... Yo casi apostaria por grandes urbes, con transportes publicos concurridos y turistas, llamame loco.
( Si no lo sabes, vitoria es bastante bonito, un ejemplo claro de la aquitectura desarrollista, y es bastante visitada, al menos por la gente del norte)
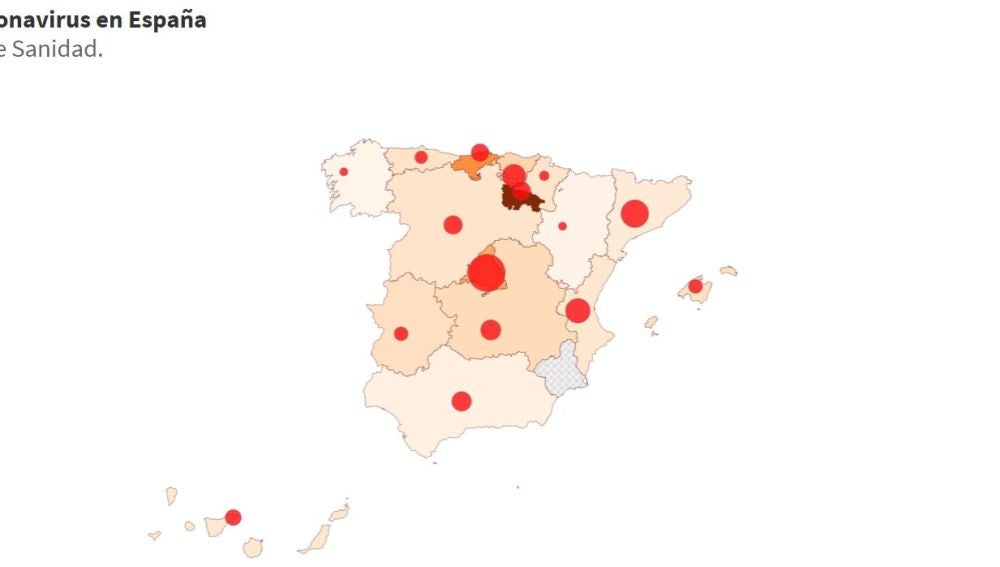
Me hace gracia que este mapa para simples este tan "trucado", que no aparece ni el punto rojo en Murcia jajajaja
| Murcia | 215 |
| Cantabria | 83 |
Casualidad que no aparezca murcia y si cantabria con muchos menos infectados... no lo se, yo vote a VOX.
Casos confirmados en España y en el mundo y claves para entender el cobi19
Adjuntos
Estoy muy loco con esta teoria (hacer click para leer hilo entero)
Y si dan con un pirado en la casa blanca o estado mayor y les vacian todos sus Ohio ahh?
Don Meliton
Madmaxista
- Desde
- 24 Oct 2016
- Mensajes
- 11.351
- Reputación
- 19.265
Y si el truco es enfermar?
Recuerdo la película de Guerra Mundial Z, cuando descubrieron que los zombies no atacaban a los enfermos y los esquivaban.
Si tenemos en cuenta que dicen que la hidroxicloroquina da muy buenos resultados a los pacientes, porque se usa para contrarestar el empuje de nuestro sistema inmunológico, pregunto yo..
Existe alguna forma de debilitar nuestro sistema inmunológico para que no reaccione tan fuerte al bichito?
Llevo viendo comentarios como este unos días.
Y cada vez que los veo, no puedo evitar pensar que creemos que la vida es una película, y que Brad Pitt va aparecer mañana con la cura del bicho.
Todos diremos, "como no lo habíamos pensado, siempre estuvo delante de nuestras narices". Y lo celebraremos con una fiesta en el planeta de los ewoks,
Mientras, en la vida real, todavía no se ha encontrado una medicación efectiva para el SIDRA o el cáncer, que no pase por dejar el sistema inmunologico para el arrastre. Asi que no se si estoy siendo pesimista cuando opino que podeis esperar a Brad sentados.
el arquitecto
sigilita
creo que ha sido en francia donde se ha testeado: Researchers Look To Old Drugs For A Possible cobi19 Treatment – It Might Just WorkImprimiros esto:
Evaluation of the Efficacy of Hydroxychloroquine in Decreasing Immune Activation in Asymptomatic HIV-infected Patients
Trump lo quiere usar...
Lo pongo pasteado por si desaparece el link..
Un forero tenía razón. Nuestro sistema inmune reacciona demasiado fuerte al bichito y es el que agrava todo.
Evaluación de la eficacia de la hidroxicloroquina en la disminución de la activación inmune en pacientes asintomáticos infectados por VIH (HCQ-01)
El estado de reclutamiento de este estudio es desconocido.
Verificado febrero de 2010
Patrocinador
del Consejo de Investigación MédicaColaboradorWellcome TrustInformación proporcionada por el (Consejoresponsable)Consejo de Investigación Médica
Identificador de ClinicalTrials.gov
NCT01067417 Recibido porprimera vez: 10 de febrero de 2010Última actualización: 29 de julio de 2010Última verificado: Febrero de 2010Historial de cambios
Propósito
Propósito
El propósito de este estudio piloto es descubrir si tomar hidroxicloroquina disminuirá la activación inmune (estimulación del sistema de defensa del cuerpo) en personas con infección temprana por VIH. La hidroxicloroquina es un medicamento que se ha utilizado con éxito durante muchos años para tratar enfermedades autoinmunes (enfermedades en las que el sistema inmunitario causa daños al cuerpo), por ejemplo, lupus y artritis reumatoide. Generalmente es seguro en el uso a largo plazo y de fácil acceso.
El sistema inmunitario se estimula en respuesta a infecciones como el VIH, por lo que los tratamientos que disminuyen la activación inmunitaria pueden tener beneficios clínicos a largo plazo, es decir, retrasar el inicio del tratamiento.
Condición Intervención Fase Infecciones por el VIH Fármaco: hidroxicloroquina
Fármaco: placeboFase 2
Tipo de estudio: Intervencionista Diseño del estudio: Asignación:
Modelo de intervención aleatoria : Asignación paralela
Enmascaramiento: Triple (Participante, Proveedor de atención, Investigador)
Propósito principal: TratamientoTítulo oficial: Evaluación de la eficacia de la hidroxicloroquina en la disminución de la activación inmune en pacientes infectados por VIH asintomáticos
Detalles adicionales del estudio proporcionados por el Medical Research Council:
Medidas de resultado primarias
- Cambio en la activación de células T CD8 en la semana 48 en comparación con la línea de base (como se muestra por un porcentaje de las células que expresan CD38 + y HLA-DR +). [Marco de tiempo: semana 48]
Inscripción: 83 Fecha de inicio del estudio: Junio de 2008 Fecha estimada de finalización del estudio: Febrero de 2011 Fecha estimada de finalización primaria: Febrero de 2011 (fecha final de recopilación de datos para la medida de resultado primaria)
Elegibilidad
Brazos Intervenciones asignadas Comparador activo: hidroxicloroquina Fármaco: Hidroxicloroquina
Tomado por vía oral 2x200mg cápsulas una vez al día durante 48 semanas.Placebo Comparator: Placebo Fármaco: placebo
Tomado por vía oral 2 cápsulas de 200 mg una vez al día durante 48 semanas
Elegibilidad
Criterios
Edades elegibles para estudio: 18 años a 65 años Sexos elegibles para estudio: Todos Acepta Voluntarios Saludables: No
Criterios de inclusión:
- Infección documentada por VIH en ELISA y prueba confirmatoria.
- Edad 18 a 65 años.
- Sin tratamiento previo a la terapia antirretroviral o sin TAR durante al menos 12 meses antes del ingreso al estudio.
- Recuento de células T CD4 superior a 400 células / µL en el análisis de sangre de detección y en otra prueba realizada dentro de los 6 meses previos a la detección.
- Carga viral de ARN del VIH en plasma superior a 1000 copias / ml en análisis de sangre
- Dispuesto y capaz de proporcionar un consentimiento informado por escrito.
- Criterio de exclusión:
- Antecedentes de psoriasis, porfiria cutánea tardía, epilepsia, miastenia gravis, miopatía de cualquier causa, arritmias cardíacas, deficiencia de glucosa 6-fosfato deshidrogenasa (G6PD).
- Diabetes mellitus insulinodependiente o no insulinodependiente.
- Enfermedad hepática crónica de cualquier causa o alcoholismo.
- Infección primaria por VIH dentro de los 12 meses previos a la detección, ya sea confirmada (prueba de anticuerpos contra el VIH negativa anterior dentro de los 12 meses) o sospechada (síntomas que sugieren fuertemente la enfermedad de seroconversión del VIH dentro de los 12 meses anteriores y no se sabe que el paciente sea positivo para anticuerpos contra el VIH antes de la prueba) enfermedad).
- Neumonía, meningitis, septicemia o cualquier otra infección grave en los 2 meses previos a la detección.
- Cualquier infección aguda con fiebre y síntomas sistémicos en las últimas 24 horas.
- Cualquier banderilla en los 2 meses previos a la selección.
- Neoplasia maligna activa (los pacientes son elegibles si el tratamiento de la neoplasia maligna se completó más de 2 años antes de la detección y no ha habido evidencia clínica posterior de enfermedad activa) o alguna enfermedad inflamatoria o mediada por el sistema inmunitario activo.
- Cualquier intento de suicidio conocido (en cualquier momento en el pasado) o antecedentes actuales o pasados de depresión que requieran tratamiento dentro de los 2 años previos a la detección. Los pacientes que no hayan tenido depresión en los 2 años anteriores pero que hayan tenido depresión en el pasado pueden incluirse si, en opinión del médico, la naturaleza del episodio anterior de depresión y el estado psicológico actual del paciente indican que el riesgo de Es probable que la recurrencia de la depresión durante el ensayo sea baja. Los pacientes que han recibido medicamentos antidepresivos por razones distintas a la depresión sintomática pueden incluirse en el ensayo.
- Una mujer que actualmente está embarazada o amamantando.
- Una mujer en edad fértil que planea quedar embarazada durante el curso del estudio, o no está dispuesta a tomar la anticoncepción adecuada (incluida la anticoncepción de barrera) durante todo el curso del estudio.
- Uso de corticosteroides sistémicos u otros medicamentos inmunomoduladores dentro de los 12 meses previos a la detección.
- Uso actual de medicamentos con efectos hepatotóxicos graves conocidos o interacción conocida con hidroxicloroquina.
- Evidencia de defectos de conducción cardíaca o arritmia cardíaca en el ECG de detección.
- Retinopatía o cambios en el campo visual detectados en el examen ocular de detección.
- Antígeno de superficie de la hepatitis B (HBsAg) positivo o positivo para la PCR de la hepatitis C (los pacientes con anticuerpos positivos para la hepatitis C pueden participar siempre que la PCR sea negativa).
- Cualquiera de las siguientes anormalidades de laboratorio en el análisis de sangre de detección:
- Hemoglobina inferior a 10,5 g / dl,
- Recuento absoluto de neutrófilos inferior a 1.0x109 / L
- Recuento de plaquetas inferior a 100 X 109 / L
- ALT o AST, o fosfatasa alcalina por encima de 2.5 x límite superior de la normalidad (ULN)
- Creatinina sérica mayor de 1.5xULN
- Liquidación estimada de creatinina (ecuación de Cockcroft-Gault *) por debajo de 60 ml / min
- Incapacidad para asistir o cumplir con el tratamiento o la programación de seguimiento.
- Participación actual en cualquier otro ensayo de intervención clínica.
contactos y ubicaciones
Contactos y ubicaciones
Elegir participar en un estudio es una decisión personal importante. Hable con su médico y sus familiares o amigos sobre la decisión de unirse a un estudio. Para obtener más información sobre este estudio, usted o su médico pueden comunicarse con el personal de investigación del estudio a través de los Contactos que se proporcionan a continuación. Para obtener información general, consulte Información sobre estudios clínicos .
Consulte este estudio por su identificador ClinicalTrials.gov: NCT01067417
Patrocinadores y Colaboradores
Consejo de Investigación Médica
Wellcome Trust
Más información
Más información
Palabras clave proporcionadas por el Consejo de Investigación Médica:
Fiesta responsable: Dr. Nick Paton Investigador Jefe nip@ctu.mrc.ac.uk, Unidad de Ensayos Clínicos del Consejo de Investigación Médica Identificador de ClinicalTrials.gov: NCT01067417 Historia de cambios Otros números de identificación del estudio: HCQ-01 2007-005057-36 Estudio recibido por primera vez: 10 de febrero de 2010 Última actualización: 29 de julio de 2010
Hydroxychloroquine
Chloroquine
Infección por VIH
Síndrome de inmunodeficiencia adquirida Síndrome de
activación inmunitaria tratamiento de
inflamación progresión de la enfermedad
ingenua Otros términos relevantes de MeSH: Infecciones por VIH Hydroxychloroquine ClinicalTrials.gov procesó estos datos el 19 de marzo de 2020 Esta información es proporcionada por ClinicalTrials.gov .
While unpublished yet, the first patient trial of Plaquenil for el bichito, conducted in Marseilles, France, has reported encouraging early results. The trial, announced in a video on Monday, was led by Didier Raoult, a physician-scientist who has published on microbes for several decades.
According to a draft article by Raoult’s team and obtained by me, 36 patients were enrolled in the trial, including 16 infected controls and 20 treated patients. The test group was given 600 mg daily of Plaquenil, which is on the WHO’s List of Essential Medicines and has been used for malaria, rheumatoid arthritis and lupus.
At day three, the study reported, 50 percent of the treated group turned from positive to negative for the el bichito bichito.
By day six, 70 percent tested negative.
As intriguing, of the 20 test patients, six who were treated with both Plaquenil and the antibiotic azithromycin did even better, the team reported. Five of the six, or 83 percent, tested negative at day three. All six, 100 percent, tested negative at day six.
Meantime, the control patients largely stayed sick longer. On days three and six, just 6.3 percent and 12.5 percent, respectively, tested negative. The research paper did not include how they were alternatively treated.
lo hicieron público el lunes o el martes, ya lo están usando en pacientes, según contaba lowfour esta tarde
también el retroviral ese, lo pone en el mismo artículo, parece que se pueden salvar muchas vidas si es cierto que funciona como parece
frangelico
Madmaxista
- Desde
- 26 Nov 2014
- Mensajes
- 40.056
- Reputación
- 123.715
La toxicidad retiniana es uno de los mayores problemas , eso es cierto.La hidroxicloroquina, si te pasas de dosis durante mucho tiempo, da pérdida visual.
Hidroxicloroquina (Plaquenil)
La hidroxicloroquina, por lo general, se tolera muy bien y los efectos secundarios graves son poco frecuentes. Los efectos secundarios más comunes son náuseas y diarrea, que suelen mejorar con el tiempo o al tomar el medicamento con las comidas. Entre los efectos secundarios menos comunes se encuentran erupciones cutáneas, cambios en el pigmento de la piel (como oscurecimiento o puntos neցros), en el cabello (decoloración o fragilidad) y debilidad muscular.
En muy pocos casos, la hidroxicloroquina puede provocar anemia en algunos pacientes. Esto puede suceder en personas con una afección conocida como deficiencia de G6PD o porfiria.
En casos poco frecuentes, la hidroxicloroquina ha causado trastornos visuales o pérdida de la visión, pero estos problemas se producen con mayor frecuencia en los pacientes que toman dosis altas durante muchos años, en personas de 60 años o mayores, o en los que sufren enfermedades renales considerables. La dosis utilizada hoy en día es menor que la que se empleaba originalmente para tratar la artritis o malaria. En la dosis actual recomendada, es muy improbable que se presenten problemas visuales durante el tratamiento con este medicamento.
Abstenuto
Madmaxista
- Desde
- 28 May 2011
- Mensajes
- 6.213
- Reputación
- 22.393
¿Podrías poner link?A ver... De cada 5 enfermos de bitxo que necesitan respiración asistida, 3 mueren y 2 quedan con capacidad pulmonar reducida. Y eso después de un mes de usar las máquinas. Me parece que no es la estrategia en la que hay que invertir. Sobre todo en comparación con los testeos rápidos a toda la poblacion.
Gracias
tunante
Madmaxista
- Desde
- 7 Jul 2006
- Mensajes
- 7.321
- Reputación
- 15.861
Hay que ser iluso para decir lo que dice en la primera frase.
Todo lo demás es razonable o debatible. Pero priorizar la economía a las vidas humanas, es de ser un sociópata más como el resto de nuestra clase política
A esto está nuestra clase política....se habla mucho de economía, pero muy poco de crisis sanitaria. ¿donde está el aluvión de medidas para paliar las carencias sanitarias?
GOOOOLFOS, ME TENEIS HASTA LA platano UNOS Y OTROS
Locoderemate
Madmaxista
- Desde
- 17 Dic 2014
- Mensajes
- 10.091
- Reputación
- 16.024
Cuál es tu p
Cuál es tu provincia?Fuera coñas, y quitando alarmismos simples, los que no sois de madrid,barcelona o vitoria veis vuestras comunidades jodidas?, lo digo porque ne la mia 1 muerto, 1 en la UCI, y por lo que he visto unas cuantas parecido.
Lo digo por si conoceis medicos en vuestra comunidad o provincia, porque en la mia me han dicho que tienen menos trabajo que nunca, no, no es trol ni coña, es la verdad, lo unico bueno que la gente deja de ir por cosas a urgencias.
King Almorta
Madmaxista
- Desde
- 13 Mar 2020
- Mensajes
- 1.933
- Reputación
- 18.439
Menos de la que imaginanaquí hay ruido de sables.
Están retando al ejército
Por razones que no hacen al caso soy miembro de una asociación de afectados por una enfermedad. Desde hace tiempo observo un uso político de la misma por ciertos contenidos que se vuelcan en su grupo de WhatsApp. Pues fíjate tu que casualidad que tiempo les ha faltado para colgar la gaita del escudo social.
No he podido contenerme y les he puesto el tweet de R2D2 alabando a Milá cuando hacían coñas de la gripecilla.
Imagino que me echaran, pero me la rezuma.
Ni olvido, ni perdón.
Similar threads
- Respuestas
- 12
- Visitas
- 525
- Respuestas
- 3
- Visitas
- 390
- Respuestas
- 3
- Visitas
- 950
- Respuestas
- 4
- Visitas
- 389
- Respuestas
- 47
- Visitas
- 3K
Compartir: