Lo que me parecía algo raro era escuchar tan pocas voces autorizadas desde el mundo de la ciencia o la medicina que llamaran a la prudencia médica, especialmente cuando empezó la vacunación de adultos jóvenes y de mediana edad. Me inquietaba la constante equiparación de estas banderillas con las desarrolladas con tecnologías tradicionales, algo que estaba implícito en cada uno de los mensajes que se transmitían a la población cuando se rozaba muy tangencialmente la cuestión de la seguridad.
Mi extrañeza aumentó cuando leí
esta noticia en enero.
Ya no sólo es que la FDA limitara a 6 meses el seguimiento de efectos adversos graves (EAG) como bien dicen los funcionarios del Servicio Navarro de Salud (puede verificarse
aquí), sino que, al permitir la agencia reguladora la vacunación del grupo placebo, se abortaba prematuramente la evaluación controlada de los mismos.
Si tenemos en cuenta de que hablamos de voluntarios que no padecían la enfermedad y que tenían medios para protegerse de la misma, las razones éticas esgrimidas para vacunarles son absolutamente injustificadas en un estudio de tal importancia.
¿Qué hubo detrás de esa incomprensible decisión, precedida de una extraña historia en que los voluntarios del ensayo clínico (que han firmado unas condiciones que deben cumplir) iniciaron una serie de protestas reclamando ser banderilleados?
Ver archivo adjunto 907086
Alcanzo a entender la necesidad de la aprobación de emergencia de las banderillas dada la elevada mortalidad que estaba causando la esa época en el 2020 de la que yo le hablo en personas mayores y otros con perfiles de riesgo alto pero, ¿cuál es la razón para limitar a sólo 6 meses la evaluación de efectos adversos graves cuando en otras banderillas de ARNm o vector viral esta evaluación suele durar varios años sumando las fases? Muestro tres ejemplos
Esta banderilla de Janssen de vector viral contra el ébola. Más de 3 años de seguimiento para evaluar efectos adversos graves.

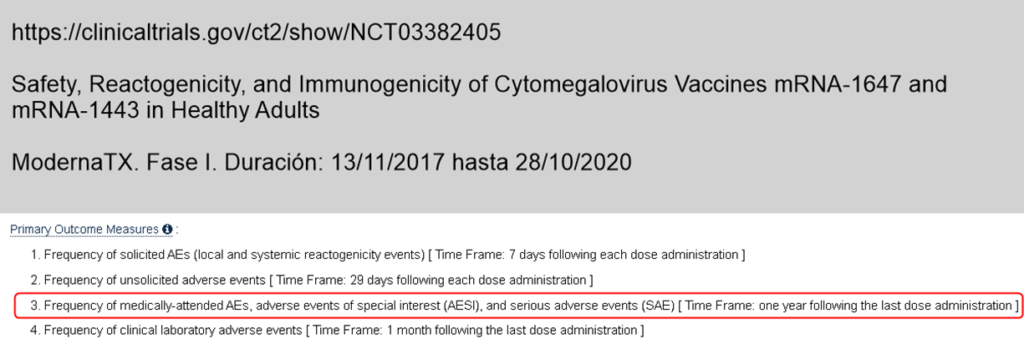
Un año de seguimiento de efectos adversos graves (SAE) en la fase I de
esta banderilla de ARNm de Moderna contra el citomegalovirus.
Y otro año para vigilar y evaluar la ocurrencia de efectos adversos graves en el
estudio de fase II de la misma banderilla.
 ¿Cómo es posible afirmar que las banderillas son seguras cuando no se han evaluado ni se van a evaluar efectos adversos graves más allá de 6 meses de forma controlada como sí se exige con banderillas desarrolladas con la misma tecnología?
¿Cómo es posible afirmar que las banderillas son seguras cuando no se han evaluado ni se van a evaluar efectos adversos graves más allá de 6 meses de forma controlada como sí se exige con banderillas desarrolladas con la misma tecnología?
Todavía resulta menos comprensible la decisión de limitar a 6 meses la evaluación de efectos adversos graves si pensamos que desde un primer momento la idea era vacunar a toda la población adulta (que incluye millones de personas con perfiles de riesgo bajo o muy bajo) para alcanzar la inmunidad de rebaño.
Para ampliar lo expuesto en este apartado recomiendo encarecidamente leer
esta publicación de Peter Doshi, editor del BMJ y Profesor de Investigación sobre Servicios Farmacéuticos de Salud, enriquecida con todo tipo de referencias. Reproduzco un interesante fragmento de la sección “Seis meses: ¿son suficientes?”.
“Una aprobación basada en seis meses de datos representaría una de las más rápidas para una nueva banderilla en la historia de la FDA. Entre las seis banderillas » pioneras en una enfermedad» aprobadas por la FDA desde 2006, los ensayos pivotales previos a la autorización tuvieron una duración media de 23 meses, según un análisis reciente.9
Seis meses también parecen ser sustancialmente más cortos que las expectativas previamente conceptualizadas. Un grupo de expertos de la Organización Mundial de la Salud sobre banderillas contra el el bichito-19 (que incluía a reguladores de la FDA) pidió en agosto de 2020 un seguimiento «hasta al menos el mes 12, o hasta que se despliegue una banderilla eficaz a nivel local».
10 Otro grupo, compuesto por autores de la industria y del mundo académico, escribió de forma similar en octubre de 2020: «recomendamos un seguimiento a más largo plazo de todos los participantes… durante al menos un año después de la aleatorización».
11’’



